认 证:工商信息已核实
访问量:3009790

大昌华嘉科学仪器部 2020-07-15 点击6296次
固体材料表面的精确表征在材料的研究和许多工业产品开发过程中起着至关重要的作用。材料表面的润湿性在油漆、印刷和生物材料与细胞间相互作用等研究领域中同样是一种非常重要的表征参数。可通过测量液体与固体材料间的接触角来表征材料的润湿性。
表面自由能基本理论
著名的杨氏方程描述了固-液-气三相接触的平衡。具体公式如下:
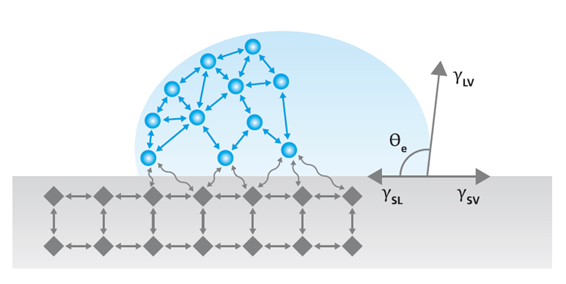
图1 固液气三相点很
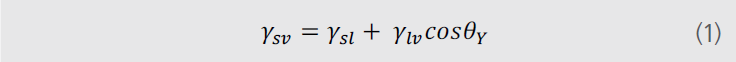
界面张力γsv、γsl和γlv构成平衡,润湿接触角,即杨氏接触角θY。杨氏方程假定固体表面化学均一且光滑,如果实际样品表面有一定粗糙度,则可以使用粗糙度校准接触角来进行表征,具体方法会在后面的文章中指出。
接触角的一个重要的应用是通过测量接触角能够计算出固体的表面自由能。表面自由能与液体的表面张力的单位均为mN/m(=dynes/cm)。尽管接触角本身能够表征材料表面的润湿性,但接触角的结果与测试的液体有很大关系。
在(1)方程中,表面自由能是通过材料的接触角、液体表面张力和固液之间的界面张力计算得到的。前两者很容易在实验中获得,关键的问题是固液间的界面张力不容易直接测得。为了解决方程中的这个问题,必须要进行一系列假定。关于表面自由能的一系列假定应运而生。
吸附和附着
为能供更清晰的理解不同的理论,必须首先解释下“粘附功”的概念。热力学粘附是指将表面分成两个新表面所需要的功,如图2所示。粘附功方程如下:
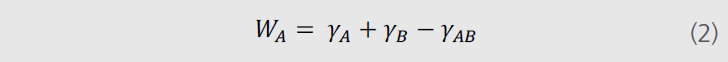
方程(2)中的γAB为两相间的界面张力,γA为A相的表面张力,γB为B相的表面张力。如果其他相为固体或者其他液体,方程则改写成如下形式:
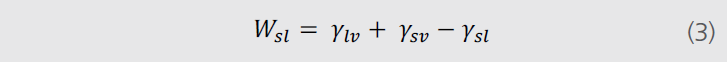
方程(1)和方程(3)何以合并成如下方程:

用同样的方法附着功的定义如图2所示。

Berthelot在19世纪末zui先使用表面自由能的计算方法。他假定固体和液体之间的粘附功(WA)等于固体附着功和液体附着功的几何平均值。
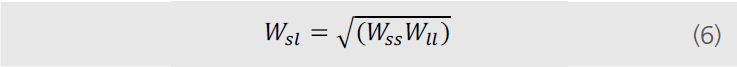
将方程(4)、方程(5)和方程(6)结合
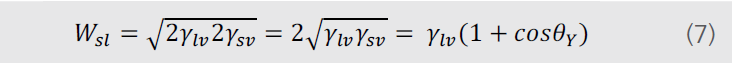
Berthelot的理论背景为分子间的伦敦作用力,因此表面自由能理论主要遵循的是超临界流体理论。
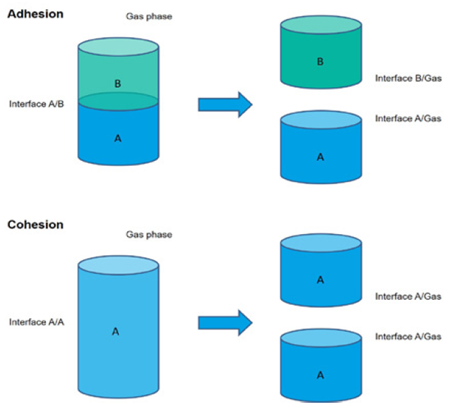
图2粘附和附着
表面自由能计算模型
表1 表面自由能方法总结
OWRK/Fowkes
将表面自由能划分成不同组分的想法假定了固液间界面张力数值取决于测试的固体样品和液体的种类。Fowkes假定固体的表面自由能(液体的表面张力)是单独部分的总和。
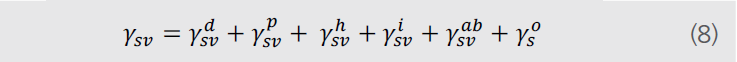
γsvd、γsvp、γsvh、γsvi和γsvab分别是色散、极性、氢、感应和酸碱部分。γso表示所有其他的相互作用。Fowkes主要是针对于仅仅含有色散部分的多种物质(固体和液体)。根据Fowkes色散作用与伦敦力的作用是由电子偶极引起的波动。Owen和Wendt跟随Fowkes的想法继续进行阐述方程(8)中除去γsvd外的所有组分都可以定义为极性部分,进而产生出方程(9)。
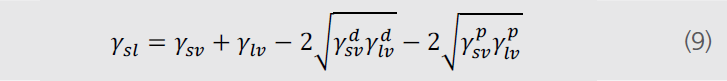
如果将方程(4)与上述方程结合,则改写后的方程称为WORK。

方程(10)中有两个未知项γsvd和γsvp,需要色散和极性组分已知的两种液体来解决这个问题。测试时需选择主打极性和主打色散部分的两种液体。水、甘油和甲酰胺可作为极性液体,二 碘 甲 烷和α-溴萘可作为色散液体。水很显然极性数值很大,可以满足使用并且是无污染的液体。对于sesame那部分的液体的选择相对来说会更复杂一些。大部分色散液体的表面张力很低,在大部分固体表面的接触角数值几乎为0°。因此需要更加特殊的液体探针。OWRK模型是最为常用的表面自由能计算模型。

Wu
Wu模型受到Owen和Wendt的影响,也将表面自由能分成极性部分和色散部分。Wu模型并没有使用几何平均数(10)计算而是使用了调和平均数(11)进行计算的。
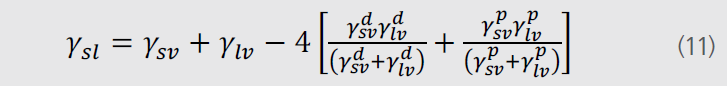
如果将方程(11)与方程(4)结合则方程可改写成如下形式:
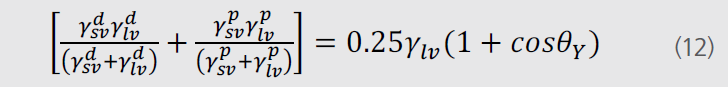
Wu方法需要至少两种液体进行测试,一种极性液体一种色散液体,最常用的仍然是水和二 碘 甲 烷。
Wu方程的主要依据来源于理论熔融聚合物的实验测量。
Wu修正了几何平均数中忽视的极性间的相互作用。

Acid-base
Acid-base模型是近期兴起的表面自由能计算模型。Van Oss,Good和Chaudhury三者提出表面自由能可分为远距离的范德华力相互作用和短距离的极性相互作用。随后,相同的作者也指出,尽管大部分极性作用是发生在临近分子之间,能够通过吸引来改变分子顺序,可改变几个结合分子的直径。可以明确一点,是使用上标A和B来代替路易斯酸碱的相互作用。通过使用Acid-base 模型方程如下所示:
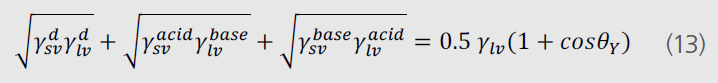
由上述可以看出长距离范德华力与色散作用相同。
上述方程(13)中有三种不确定项,因此需要三种液体进行测试,1种色散液体和2种极性液体。
在分别介绍将极性组分分成电子供体和电子受体后,就很容易理解许多有机高分子材料尤其是极性生物高分子,主要或者只是电子供体或者极少部分仅仅是电子受体。表面仅仅是电子供体或者电子受体则叫做单一极性。这样的单一极性表面有许多意想不到的性质,可以解释一些难以理解的胶体和表面的现象。Acid-base模型能够提供稳定的测试结果。
使用Acid-base理论的难点是没有任何已知酸碱组分的液体。可估计酸碱比率,极性部分可使用接触角方法测定,如甘油和甲酰胺滴在单一极性的表面如PMMA。
针对该模型的主要争议在于酸性和碱性组分的界面张力值很有可能是负值。色散部分不能够小于0,但如果是酸碱组成条件是确定的情况下也有可能是0。由此则会引发一个讨论:如何选择测试液体,下列液体均可使用,水,甘油,二 碘 甲 烷,甲酰胺和α-溴萘。
Schultz 1&2
Schultz模型能够满足高能表面的表面自由能的计算。尽管从方法角度来说之前说的方法也可以使用,但问题在于高能表面采用接触角方法很可能数值很低或者接近于0。在这种情况下很小的误差会使结果有很大偏差。出于这种原因Schultz模型指出了需要将固体浸润到其他液体里面再用其他液体进行接触角测试。
Schultz模型还可分成两种模型,Schultz1和2。Schultz1是将固体浸润到非极性液体里面再用极性液体进行接触角的测试,Schultz2则与Schultz1完全相反,使用捕泡法进行接触角的测试,如图3所示。
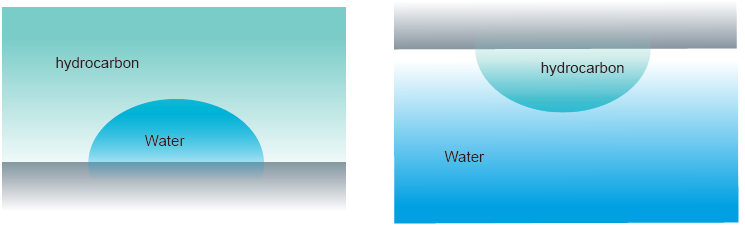
图3 左边为Schultz1,右边为Schultz2
由于接触角测试过程中有两种液体的存在,需要考虑液体和固体之间的相互作用。
碳氢化合物和固体之间的相互作用可写作如下方程:
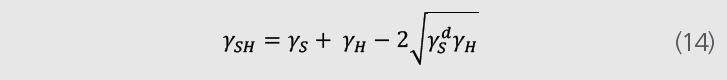
S=固体,H=碳氢化合物。由于碳氢化合物没有记性组分,那么极性作用为0。
水和固体间的相互作用可写成如下形式:

W=水。
固液气三者使用的杨氏方程如下所示:
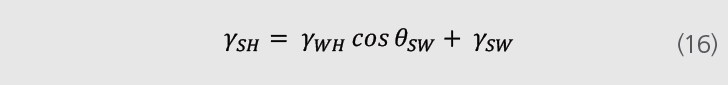
将方程(14)(15)和(16)结合可得到如下方程:
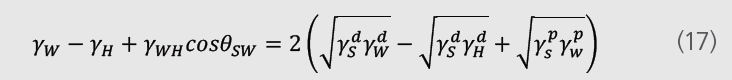
由于方程中包含水和碳氢化合物间的界面张力,该数值需要测定得到。
Schultz主要针对于高能固体表面,如金属、金属氧化物和玻璃等。
EOS模型
尽管状态方程有很多不同的形式,做广为熟知的是Neumann提出的方程,如下所示:

当中的常数β=0.0001247是通过实验确定的。该模型只需使用一种液体。针对于该模型目前也有一些争议,争议涉及到常数β是否会恒定不变的;状态方程并没有将表面张力分成不同的部分;状态方程对于测试液体的纯度要求非常高;状态方程不能够像杨氏接触角一样通过热动力学方法解释前进角。
Zisman曲线模型
Zisman模型主要针对液体和固体间接触角接近0°的情况。表面张力的数值与表面自由能不同的是,并没有将其分成极性和色散部分。实际上,表面张力是通过测定同一表面和不同液体之间的接触角获得的。COSθ为Y轴,表面张力是X轴。

图4 Zisman曲线模型
非理想表面的表面自由能
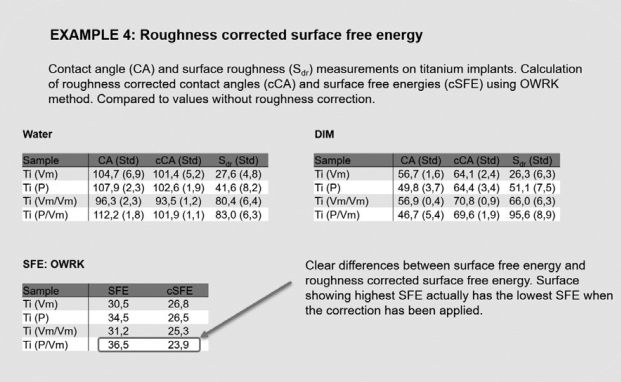
表面自由能通过杨氏方程测试的接触角来确定。杨氏方程是假定固体表面为理想表面,理想表面意味着化学和形貌均一。然而实际上很难找到理想表面,表面或多或少都会有粗糙度的。如果通过接触角计算表面自由能而没有将固体表面的粗糙度考虑进去的话,表面自由能的数值是不准确的。因此针对粗糙表面建议使用粗糙度校准接触角来计算表面自由能。
总结
本文介绍了几种常见的表面自由能模型。表面自由能可根据极性相互作用分成不同的组分。然而,仍然有很多理论上的问题需要去探讨。本文并不能够建议那种模型更好,文章开始处的表中总结了各模型的特点及优点。在实际过程中建议如果需要数据比对的话,尽量使用同一种模型进行表面自由能的计算。
更多内容,关注“大昌华嘉科学仪器部”微信公众号



